李宁宁医生的科普号
- 精选 常见化疗不良反应的护理
一、白细胞/中性粒细胞减少 1、经常开窗换气以保持室内空气清新。 2、外出戴口罩,避免到人多聚集的场所。 3、每日三餐后用西吡氯胺漱口水清洁口腔,可以有效的预防口腔感染。 4、每晚坚持高锰酸钾坐浴是
 李宁宁 主治医师 北京协和医院 肿瘤内科5575人已读
李宁宁 主治医师 北京协和医院 肿瘤内科5575人已读 - 临床试验招募 涎腺肿瘤患者招募
HER2表达的局部晚期或转移性涎腺肿瘤招募1、试验简介评价注射用维迪西妥单抗治疗HER2表达的局部晚期或转移性涎腺肿瘤患者的疗效及安全性的Ⅱ期临床研究预计共招募受试者10例患者2、面向患者HER2中高表达(IHC2+、3+)的初治或既往接受过系统性抗肿瘤治疗后进展的局部晚期或转移性涎腺恶性肿瘤患者.3.入组标准1.自愿同意参与研究并签署知情同意书;2.男性或女性,年龄≥18岁;3.预期生存期≥12周;4.具有组织病理学确诊的无法接受手术完全切除的局部进展或转移性涎腺恶性肿瘤;5.确诊为无法手术切除的局部进展或转移性涎腺恶性肿瘤后,未接受过全身抗肿瘤治疗的受试者;或既往接受过至少一线系统性治疗后出现疾病进展,这其中患者接受过新辅助或辅助化疗方案治疗后12个月内出现疾病进展,可以入组该临床研究;6.具有RECISTv1.1标准规定的可测量病灶;7.受试者能够提供HER2检测的肿瘤原发或转移灶部位标本;HER2IHC为2+或3+;8.ECOG体能状况评分0-2分;9.足够的心、骨髓、肝、肾功能(以研究中心正常值为准):1左室射血分数≥50%;2血红蛋白≥9g/dL;3绝对中性粒细胞计数(ANC)≥1.5×109/L;4血小板≥100×109/L;5无肝转移者,血清总胆红素≤1.5倍正常值上限(ULN);有肝转移者血清总胆红素≤3×ULN;6无肝转移时,ALT和AST≤2.5×ULN,有肝转移时ALT且AST≤5×ULN;7血肌酐≤1.5×ULN;10.对于女性受试者:应为手术绝育、绝经后的患者,或同意在研究治疗期间和研究治疗期结束后6个月内至少采用一种经医学认可的避孕措施(如宫内节育器[IUD],避孕药或避孕套),在研究入组前的7天内血清或尿妊娠试验必须为阴性,且必须为非哺乳期。男性受试者应同意在研究治疗期间和研究治疗期结束后6个月内至少采用一种经医学认可的避孕措施(如避孕套、禁欲等);11.愿意且能够遵从试验和随访程序安排。联系方式:15510583113
李宁宁 主治医师 北京协和医院 肿瘤内科192人已读 - 就诊指南 Kras突变抑制剂临床研究招募
JAB-21822-1002研究招募广告 剂量递增阶段 尊敬的患者朋友: 一项JAB-21822用于KRAS p.G12C突变的晚期实体瘤的I/II期临床研究正在北京协和医院开展。本研究已经经过了国家药品监督管理局的审评,并已经通过了本院伦理委员会的批准。JAB-21822试验药物尚未获批上市,现面向社会招募晚期实体瘤患者。 JAB-21822是一种KRAS p. G12C共价抑制剂,可以将KRAS p. G12C锁定在非活化状态,阻断KRAS向下游的信号转导,从而发挥抗肿瘤作用。 目前,本研究处于1期阶段,用于确定JAB-21822作为口服单药治疗KRAS p.G12C突变的晚期实体瘤的安全性和耐受性,并确定2期研究推荐剂量(RP2D)。 招募条件: 1. 年龄≥18岁; 2. 患有组织学或细胞学确诊为局部晚期或转移的、经标准治疗失败或缺乏标准治疗的晚期实体瘤受试者,优先入组有KRASp.G12C突变的实体瘤; 3. 能提供既往肿瘤组织标本或新鲜的肿瘤组织标本; 4. 实体瘤患者必须具有至少一个符合RECISTv1.1定义的可测量的病灶; 5. ECOG评分0-1分; 6. 既往未使用过KRASp.G12C抑制剂治疗的。 * 最终入选标准由临床医生评估,并以您的全面体检结果为准。 如果您参加此项研究,您需要配合的事项有: 按照试验要求服用研究药物,21天为一个治疗周期,您需要在第1和2周期第1、8和15天,第3和4周期第1和15天,以及此后每周期的第1天进行安全性访视。 招募时间:自2021年08月开始至招满为止。
李宁宁 主治医师 北京协和医院 肿瘤内科646人已读 - 就诊指南 北京协和医院肿瘤内科开展三阴乳腺癌免疫治疗联合安罗替尼对比白蛋白紫杉醇临床研究
我院正在开展一项由应红艳教授作为主要研究者的“TQB2450注射液联合盐酸安罗替尼胶囊对比注射用紫杉醇(白蛋白结合型)一线治疗三阴性乳腺癌随机、阳性药物平行对照、多中心Ⅲ期临床试验”,该研究已经通过国家药品监督管理局批准。TQB2450注射液片为注射用生物制品,用以治疗三阴性乳腺癌。 参加本研究的基本条件: 1.经组织学确诊的初诊Ⅳ期或复发/转移性、且不适合手术治疗的三阴性乳腺癌受试者; 2.未接受过其他抗血管生成类药物治疗及免疫抑制剂治疗的患者; 3. 存在RECIST 1.1标准定义的可测量病灶; 4.年满 18周岁; 5. …… 具体可进一步咨询
李宁宁 主治医师 北京协和医院 肿瘤内科3379人已读 - 就诊指南 协和医院肿瘤内科临床研究招募中
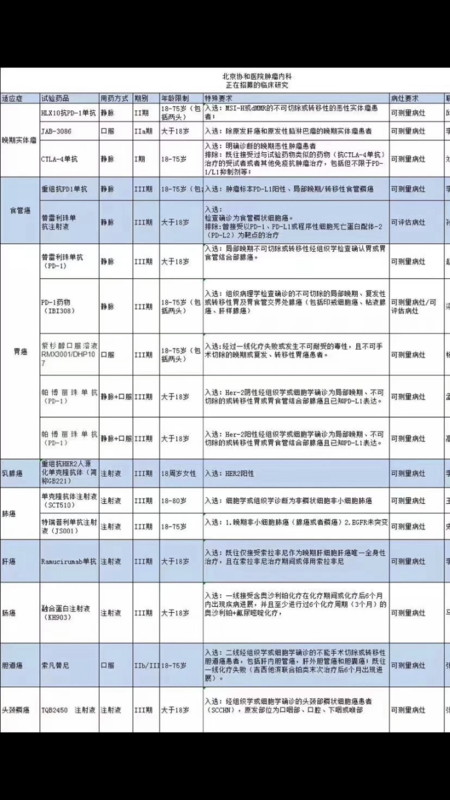 李宁宁 主治医师 北京协和医院 肿瘤内科2430人已读
李宁宁 主治医师 北京协和医院 肿瘤内科2430人已读 - 就诊指南 北京协和医院肿瘤内科招募 HER2 阳性转移性乳腺癌 临
尊敬的患者,您好: 我们正在中国展开一项国际III期临床研究,旨在测试一种赫赛汀生物类似物对首次乳腺癌复发或者转移的男性或女性患者的疗效。 本临床试验已经获得中国食品药品监督管理局(批准文号:2015L01326)和医院伦理委员会的批准。 如果您(或者您认识的某人) 符合下列条件,将有可能参加本研究: 1.年龄 ≥18 的男性或女性; 2.经组织学和/或细胞学确诊的乳腺腺癌且HER2过量表达 3. 患者既往未对复发或转移性疾病进行过全身性化疗、生物或靶向药物治疗 4. 诊断为复发性(局部或转移性)疾病前至少12个月停止使用既往含曲妥珠单抗和/或拉帕替尼的新/辅助疗法(即无疾病间期≥12个月)。如果未使用曲妥 珠单抗/拉帕替尼,必须在诊断为复发性(局部或转移性)疾病前至少6个月 (即,无疾病间期≥6个月)停止使用紫杉烷的新/辅助治疗 您的医生还会根据其他医学标准进行检查,以确定您是否适合参与本研究。本研 究需要您按照方案前往研究中心进行访视,以便研究医生和护士能够监测您的整 体健康状况。 临床试验期间,您将接受免费的研究药物/对照药治疗。在您参与本研究期间,您会获得研究医生对您疾病的科学指导,对您身体状况的密切医疗监测与免费接受试验方案所列的检查。我们会采取措施尽量降低上述这些研究操作带来的影响和布什。
李宁宁 主治医师 北京协和医院 肿瘤内科2528人已读 - 就诊指南 开展晚期或不可切除的局部晚期胃癌一线研究
2017-10-20 GCP小行家 入选标准: 1)签署书面知情同意书 2) 受试者必须患有无法手术治疗的晚期或转移性GC或GEJ癌且组织学检查证实主要为腺癌。 3) 受试者必须从未接受过全身治疗(包括HER 2抑制剂)作为其晚期或转移性疾病的主要治疗方案。 4)允许的既往治疗: 既往接受GC或GEJ癌辅助或新辅助化疗、放疗和/或化放疗的受试者,如果既往方案最后一次治疗发生于随机前至少6个月,允许入选。允许进行姑息性放疗,必须在随机分组前2周完成。 已经获得批准的具有抗肿瘤适应症的中医药末次给药在随机前2周完成。 5) 受试者必须有至少一个按照RECIST 1.1标准,通过CT或MRI可测量的病灶或可评价疾病;影像学肿瘤评价应在随机前28天内进行。 6) ECOG体力状态评分为0或1分。 7) 必须提供用于生物标志物分析的肿瘤组织。肿瘤组织标本必须是新鲜的或是在招募前6个月内获得的存档样本,在获得样本后可能不会进行全身治疗(如辅助治疗)。组织必须是空心针穿刺、切除或切开的活检标本。 8) 实验室筛查值必须符合一定标准 9) 男性或女性,年龄≥ 18岁 10) 女性必须是非哺乳状态。 排除标准 1. 目标疾病例外情况 a) 已知为Her2阳性状态 b) 有已知的未经治疗的CNS转移的受试者。如果受试者CNS转移经过充分治疗,并且随机前神经学指标恢复至基线(不包括与CNS治疗有关的残留体征或症状)至少2周,其有资格入选。此外,受试者必须在随机前停用糖皮质激素,或接受稳定或减量中的每天剂量≤ 10 mg的强的松(或等效剂量)至少2周。 c) 通过适当干预无法控制腹水的受试者。 2. 病史和伴随疾病 a) 在过去3年内出现活动性恶性肿瘤,已明显治愈的局部可治愈癌除外,例如基底或鳞状细胞皮肤癌、浅表性膀胱癌或前列腺、宫颈或乳腺原位癌。 b) 出现活动性、已知或疑似自身免疫性疾病的患者。允许I类糖尿病、自身免疫性甲状腺炎引起的残留甲状腺功能减退症(只需使用激素替代疗法)或无需进行全身治疗的皮肤疾病(例如,白癜风、银屑病或脱发)受试者入组。 e) 在给予研究药物14天内需要使用皮质类固醇(> 10 mg/日强的松等效剂量)或其他免疫抑制药物进行全身治疗的受试者。如果没有活动性自身免疫性疾病,允许使用吸入性或局部类固醇激素,或每天> 10mg强的松等效剂量的肾上腺激素替代治疗。 d) 既往接受过抗PD-1、抗PD-L1、抗PD-L2、抗CD137或抗CTLA-4抗体,或任何其他以T细胞共刺激或检查点通路为靶点的抗体或药物治疗。 e) 在给予研究药物之前,除了听力损失、脱发和疲劳外,既往抗癌治疗引起的所有毒性必须已恢复至1级(NCI CTCAE第4版)或基线水平。 f) 受试者有>1级周围神经病变。 g) 研究者认为可能会增加与参加研究、研究药物给药有关的风险,或影响受试者接受研究药物的能力的任何严重的或未控制的疾病或活动性感染。 h) 已知有人免疫缺陷病毒(HIV)检验阳性病史或已知有获得性免疫缺陷综合征(AIDS)。 3. 体检和实验室检查结果 a) 任何乙型肝炎病毒或丙型肝炎病毒的检查结果阳性,乙肝表面抗原阳性,或丙型肝炎抗体阳性(除非HCV-RNA阴性)。 4. 变态反应和药物不良反应 a) 对研究药物组分有过敏或超敏反应史 b) 对化疗方案的任何研究药物有禁忌症。 5. 其他排除标准 a) 犯人或被强行监禁者(注意:在某些特定情况下,被监禁者可入选或允许继续作为受试者)。需要严格的申请且必须由百时美施贵宝批准。 b) 因治疗精神病或身体疾病(如传染病)而被强制拘禁者 6. 育龄期女性 育龄期女性(WOCBP)定义为任何已经有过月经初潮并且没有做过绝育手术(子宫切除术或双侧卵巢切除术)且还没有绝经的女性。绝经定义为> 45岁的女性在没有其他生物学或生理学原因的情况下闭经12个月。此外,为确认绝经,年龄在55岁以下的女性血清促卵泡激素(FSH)的水平必须 > 40mIU/mL。
李宁宁 主治医师 北京协和医院 肿瘤内科1789人已读 - 医学科普 靶向药物的前世今生
在目前的肿瘤治疗领域,火爆了数年还热度不减的非靶向药物莫属了!那么,到底什么是靶向药?它和化疗药物有什么不同之处?所谓靶向——它的标靶又是什么......每次当医生向您或您的家属交代治疗计划的时候,您的脑海中一定迅速闪过这些问题;今天,希望能通过小编轻松地讲解,让您对此瞬间了然吧。 在我们站到统一战线上,与肿瘤进行对抗的这场持久战中:化疗药物就像我们司令部派出去的装甲兵、坦克,这个队伍浩浩荡荡、对敌人进行无差别打击和无情地碾压,对相当多数目的肿瘤细胞敌兵有杀伤作用;当然,同时也难免对环境造成了一定的影响,这种影响就是药物的副反应,需要我们去密切监测、积极处理。而靶向药物在战争中就好像精确定位的导弹,它能够定位并识别出狡猾的敌人的补给站、运输线、甚至敌营司令部,由此进行精确、彻底的打击。 靶向治疗,其实就是指分子靶向药物;它针对的是肿瘤发生、发展过程中关键的基因、分子、甚至蛋白;阻断肿瘤细胞内赖以生长的信号通路——“溯其源、断其路、从而去其害”;它与化疗药物针对分裂迅速的细胞进行杀伤不同,它更有目标,更针对肿瘤的本质。从1960年美国费城的研究者发现部分慢性髓性白血病患者费城染色体异常,到2001年针对这个染色体的首个靶向药物的问世,这当中的曲曲折折,岂是小编这寥寥数笔,能记录得清的。这个进步,使靶向药物走进了人们的视线,随之而来的这数年,在各个瘤种中多个靶向药物的上市,给广大患者带来了更多的获益;也吸引了众多充满希冀的目光。 目前,靶向药物分为几大类:1.抗血管生成抑制剂,主要针对肿瘤血管的相关靶点;2.单/多激酶抑制剂,针对单个或多个靶点(酪氨酸激酶);多为小分子制剂,口服为主;3.细胞生长周期和凋亡的药物;4.免疫调节和联合治疗。 靶向药物有这么多分类,真是选择困难。到底该怎么选?专业的肿瘤科医生在选择您适合哪种治疗的时候,需要参考的因素可多了——您的原发肿瘤类型及部位、基因状态、基础疾病...甚至还会参考人种、吸烟史、性别等因素;听起来很复杂是不是?不同的靶向药物用法也是不尽相同,有的是静脉应用,有的是口服用药,有的与化疗药物联合收效甚好,有的只适合单独用药...就仿佛我们在战争中,需要根据不同类型的敌人、不同的斗争阵地,来选择不同的远程导弹出击,是一个道理! 目前,虽然总体靶向药物价格相对昂贵,但是已经有部分药物进入了全民医保目录,这是广大患者的福音。我们医生能做的就是根据您的情况,为您细致地评价,如果您是适合靶向治疗的患者,我们会为您建议相应的靶向药物的选择,供您参考。无论化疗、靶向、还是免疫治疗......我们一直希望,能与您携手,共抗肿瘤;愿我们与癌对抗的战场,硝烟不再;盼每一天,都是个晴天。 本文系李宁宁医生授权好大夫在线(www.haodf.com)发布,未经授权请勿转载。
李宁宁 主治医师 北京协和医院 肿瘤内科13人已购买 - 医学科普 拨云见日,教您看懂化疗后“血象”!
化疗后处于休疗期的您,是否经常攥着各医疗机构的化验报告,焦虑疑惑,无从下手?面对小小化验单上二十余项数据,该看哪一项?指标异常到什么程度需要处理?什么时候该选择求助于医生?今天,小编就带您初步解读您需
李宁宁 主治医师 北京协和医院 肿瘤内科58人已购买 - 就诊指南 胆道癌二线治疗临床研究开展
评价索凡替尼二线治疗不能手术切除或转移性胆道癌患者疗效和安全性的单臂、多中心、开放性II 期临床研究 (方案号2016-012-00CH1) 主要入选标准: 1. 年龄> 18岁; 2. 经组织学或细胞学确诊的不能手术切除或转移性胆道癌患者,包括肝内胆管癌(IHCC),肝外胆管癌(EHCC)和胆囊癌(GBC); 3. 在开始研究治疗前仅接受过1种化疗方案,且治疗失败,毒副作用不可耐受(既往接受过辅助或新辅助化疗,完成治疗6个月以内出现疾病进展/复发也可以入组); 4. ECOG体力状况 0或1分(附件1); 5. 患者有可测量病灶(根据RECIST标准 1.1版本); 6. 预期生存≥12周; 主要排除标准: 研究治疗开始前4周内接受过已获批的或在研的抗肿瘤治疗,包括但不限于化疗、根治性放疗、生物靶向治疗(无抗血管生成作用的酪氨酸激酶抑制剂除外,如经过2周洗脱期也可入组)、介入治疗、免疫治疗和抗肿瘤中药治疗(以中药说明书适应症为准,如经过2周洗脱期也可入组)等; 研究治疗开始前接受过已获批或在研的其他具有抗血管生成作用的酪氨酸激酶抑制剂(如索拉菲尼,舒尼替尼等) 或其他具有抗血管生成作用的单抗(如贝伐单抗等); 研究者确定肝脏转移灶占肝脏总体积的一半及一半以上; 肝功能(Child-Pugh改良分级法)评分>7(见方案附件3); 研究治疗开始前2周内接受过针对骨转移灶的姑息性放疗; 研究治疗开始前2周内(贯叶连翘为3周)服用过CYP3A4的强诱导剂或强抑制剂(见方案附件4); 已知有显著意义的肝病病史,包括病毒性肝炎[已知为乙型肝炎病毒(HBV)携带者必须排除活动性HBV感染,即HBV DNA阳性(>1×104/ml);已知丙型肝炎病毒感染(HCV)且HCV RNA阳性(>1×103/ml)],或其它肝炎,肝硬化; 患者入组前实施过重大外科手术(30 ml)、咯血(4周内>5 ml的新鲜血液)或者12月内发生血栓栓塞事件(包括卒中事件和/或短暂性脑缺血发作);
李宁宁 主治医师 北京协和医院 肿瘤内科1511人已读





